国际科学界如何确定新的抗病毒药物来应对Covid-19?
2021年11月5日
作者:Daren Fearon博士代表钻石光源有限公司
Covid-19大流行激发了国际合作努力,以寻找有效的抗病毒药物。基于片段的药物发现是一种完善的早期药物发现工具。同步加速器能力的进步和流线型晶体浸泡设施的引入,例如世界上第一个XChem在钻石光源的平台,在样品制备、数据收集和碰撞识别之间的吞吐量和集成方面提供了实质性的改进。计算对接等其他新技术也为国际社会应对新冠肺炎疫情做出了积极贡献。
为什么需要抗病毒药物来对抗冠状病毒?
在Covid-19大流行期间,冠状病毒戏剧性地进入了公众意识。随着大流行的形成,研究小组迅速合作开展了一系列研究,以更好地了解SARS-CoV-2病毒,并开发潜在的抗病毒药物。
尽管SARS- cov -2病毒现在已经众所周知,但在过去20年里,其他冠状病毒也引发了一些疫情,包括SARS(严重急性呼吸综合征)流行病和中东呼吸综合征(MERS)。
密切的国际伙伴关系以极快的速度研制出了有效的疫苗,目前正在全球范围内开展疫苗接种工作,但非洲、亚洲和南美洲的一些国家的疫苗覆盖率将较低。疫苗显然不能100%有效地预防感染,而且疫苗耐药菌株已经在蔓延。如果没有治疗方法,Covid-19可能会像季节性流感一样持续存在。因此,抗病毒药物将在与这种病毒的长期斗争中发挥重要作用。目前仍没有针对中东呼吸综合征的获批治疗方法,这一事实及时提醒我们必须采取紧急行动。
幸运的是,在抗病毒药物筛选方面也有了显著的国际合作,使用x射线晶体学和计算对接技术的高通量片段筛选等新技术使这项工作得以快速开展,并使数据公开传播到更广泛的科学界。其中大部分数据在发表之前就已发布,以便更广泛的科学界能够更快地在这些成就的基础上进行研究。
本文重点介绍了英国国家同步加速器、Diamond和世界各地许多其他研究小组之间最近的合作工作,这些合作增加了关于Covid-19的全球知识库和潜在抗病毒药物的开发。
图1。钻石光源(DLS)鸟瞰图(图片来源:钻石光源2020)
你知道XChem的片段筛选平台可以在不到一周的时间内筛选1000个化合物吗?
基于片段的筛选现在已经成为早期药物发现的有力方法。XChem位于钻石光源的工厂(图1)成立于2015年,是世界上第一个通过x射线晶体学提供常规中/高通量碎片筛选的工厂。类似的平台目前正在世界各地的其他同步加速器中建立。该设施为用户提供了专用的实验室设施和I04-1波束线上的同步加速器波束时间,以及本地支持和专业知识,使他们能够实施高度简化的流程,在不到一周的时间内可以单独筛选多达1000种化合物。(钻石的网站;v Delft F,翻译科学家2016)[1]。
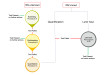
基于片段的药物发现不是从更大的基于底物的分子开始,也不是从数十万个药物大小的分子中筛选,而是从更有限的小分子或片段库开始。寻找那些可能只与目标结合微弱但有效的化学片段,并将它们结合起来生成具有有用亲和力的化合物,所需的文库比传统的高通量筛选要小得多,并且可以产生更多的命中(图2)。
图2。用于识别碎片命中的最常用生物物理技术的比较。
这种方法可以促进先导鉴定,因为小片段往往结合到蛋白质上更多的位点。此外,使用XChem提供的自动化技术直接在晶体中进行碎片筛选,使吞吐量比以前的技术快几个数量级。
一系列的新技术、新技术和新算法已经允许开发一个快速、精简的过程,包括晶体浸泡、收获、自动数据收集和低开销的数据分析。这些包括:
•声学液体分配-强大的分配化合物到特定的滴。
•图像识别-发现和选择晶体。
•机器人辅助人工收获-允许快速选择晶体。
分析衍射数据的算法-自动识别异常值并优化提取信号-平台开发了简化密度解释和细化的工具(PanDDA和XChemExplorer)。
•协同网络应用程序——允许注释和公开传播蛋白质配体复合物数据(引用Fragalysis)
•开发新的片段库(引用Keseru, Nat Comms, SpotXplorer论文)
来自100多个学术项目、30个行业项目和40多个合作项目的丰富经验意味着,XChem平台在大流行早期进行片段筛选方面处于有利地位。XChem工厂接待了许多国际研究团队,包括来自牛津大学、剑桥大学、加州大学旧金山分校和圣保罗大学的同事。
我们能识别与SARS-CoV-2蛋白结合的片段吗?
新冠肺炎合作研究项目
已经确定了一些针对SARS-CoV-2病毒的潜在药物靶点(图3),许多国际研究和Covid-19合作研究项目正在快速开展。
图3。新冠病毒的潜在药物靶点已在XChem进行筛选
由Martin Walsh团队和Diamond的XChem团队领导的一个国际团队(图4),加上以色列Weizmann科学研究所的Nir London团队,使用基于片段的筛选方法测试了近1250个片段的文库对抗SARS-CoV-2主蛋白酶(Mpro)(图5)(Douangamath, a . et al. 2020)[4]。屏幕识别了71个横跨整个活性位点的命中点,以及3个在二聚体界面的命中点。这些结构揭示了通过合并共价和非共价片段命中快速开发更有效抑制剂的途径,并为正在进行的针对SARS-CoV-2主要蛋白酶的基于结构的药物设计提供了有价值的结构和反应性信息。
图4。Diamond负责Mpro片段屏幕的团队(从左到右:Martin Walsh, Claire应变- damerell, Daren Fearon, David Owen, Ailsa Powell, Frank von Delft, Rachael Skyner, Petra Lukacik, Louise Dunnett, Alice Douangamath, Jose Brandao-Neto, Conor Wild)。
共有68个共价片段和1176个非共价片段通过共结晶或浸泡到晶体中筛选。1877个晶体被安装在Diamond,收集了1638个分辨率高于2.8 Å的数据集,并产生了与Mpro结合的96个片段的结构。这项研究于2020年2月13日首次获得蛋白质晶体,并于3月7日收集了所有实验数据,以非常快的速度完成。仅三天后,第一个晶体结构就公开了,到2020年4月初,在不断演变的大流行中,所有最终结构都被释放了。
图5。SARS冠状病毒Mpro二聚体的表面表示,XChem屏幕上的片段命中显示为黄色棒。
碎片命中如何发展成有效的抑制剂?
另一项由国际科学家组成的合作被称为COVID登月计划,旨在快速开发一种临床有效的抗病毒药物。
2019冠状病毒登月计划(II)始于2020年3月的一次自发的虚拟合作。随着各国采取封锁措施,一群科学家、学者、药物研究团队和学生开始在推特上与时间赛跑,以确定可以阻止SARS-CoV-2感染的新分子,并开发出最脆弱社区可以轻易获得的药物。
最终,超过150名科学家——包括数十名搁置自己项目的学生——加入了“登月计划”,众包分子化合物的想法,对它们进行建模,并在体外对它们进行抗病毒评估。他们的目标是:为COVID-19和相关病毒大流行提供安全、全球负担得起的非营利性口服治疗。
登月计划的创始人之一;牛津大学结构化学生物学教授、钻石光源首席光束科学家Frank von Delft在6月21日的《自然》杂志上发表了一篇关于该项目的文章;“公开药物研发的努力总是非常缓慢——我们的工作就像一列特快列车,在我们铺设的轨道上行驶,这是一种我们都没有意识到是可能的工作方式。”
“登月计划”的合作伙伴包括学术和工业集团,如英国国家同步加速器钻石光源(Diamond Light Source);魏茨曼科学研究所(以色列);牛津大学纳菲尔德医学系(英国);PostEra(美国/英国);纪念斯隆·凯特琳癌症中心(美国);包括MedChemica有限公司(英国)和被忽视疾病药物倡议(瑞士)在内的药物发现咨询公司,目前正在牵头协调建立诊所的努力,该诊所最近获得了威康公司800万英镑的资助。
该项目将来自世界各地化学家的新抑制剂设计与机器学习和机器人实验相结合。所有数据都将实时发布,以实现全球协作和快速进展(Covid Moonshot Consortium;PostEra网站)[3]。
“登月计划”的目标是SARS-CoV- 2主要蛋白酶Mpro,该蛋白酶在冠状病毒中高度保守,对病毒复制至关重要,使其成为关键的药物靶点。迄今为止,该项目涉及全球超过7000种设计和350名设计师,测试了800多种化合物,其中许多是基于在Diamond进行的原始片段筛选的结果(图6)。希望开放科学方法能够开发出许多新的工具、方法和最终可行的候选治疗方法。
图6。Covid Moonshot合作用于设计更有效的抑制剂的片段命中叠加
由于前所未有的合作,已经取得了快速进展,该团队现在的目标是在2021年底之前确定临床前候选分子,这些化合物将以药丸形式易于制造,并将通过有效抑制SARS-CoV-2病毒的主要蛋白酶(MPro)发挥抗病毒作用。该项目现在进入了资本密集的阶段:调整、优化和测试这些分子,以将它们开发成一种安全的治疗方法。
Moonshot化合物已在多个中心进行了筛选,包括Diamond XChem工厂、Weizmann研究所伦敦组(以色列Rehovot)以及Schofield组(牛津大学化学研究实验室)。
为什么科学家们瞄准Nsp3宏域?
另一个潜在的抗病毒药物靶点是来自SARS-2-CoV-2病毒的非结构蛋白3 (Nsp3)的宏结构域(Mac1)部分。Nsp3宏结构域允许病毒逃避免疫反应,对病毒复制至关重要。之前的研究表明,缺乏Mac1的病毒不能在人类细胞中复制,这表明用药物阻断它也会有同样的效果。
最近一项涉及50多个跨国合作者的国际研究使用XChem的光束线和实验室设施(图6)和加州的先进光源进行了大规模的计算对接和晶体学筛选工作,以确定主要针对该结构域活性位点的化合物。这项研究包括来自牛津大学、QCRG结构生物学联盟、加州大学旧金山分校的研究人员和XChem平台上的科学家,可能代表了针对任何公开可用的目标的高分辨率晶体碎片的最大集合。
图7。钻石光源光束线104-1实验箱显示样品变换器和样品环境。钻石光源有限公司版权所有
通过对2500多个片段的晶体学筛选,发现了234个直接与蛋白质表面感兴趣位点结合的片段化合物。所有这些晶体结构都已在公共领域发布。
研究人员独立地使用计算对接(另一种创新的药物发现技术,使用计算机模型和模拟来评估虚拟分子可能与Mac1相互作用的相互作用,以及它们作为药物发现起点的希望)筛选了超过2000万个片段(主要来自ZINC15)。在选择用于晶体学浸泡的60个最佳点击率中,有20个产生了结构,都是高分辨率的(0.94-1.01 Å)。20个实验确定的结构中的大多数证实了对接的预测。
这项研究重申了晶体学和计算筛选日益增长的重要性,无论是在为SARS-CoV-2抗病毒药物提供大量药物先导,还是在为新的计算方法提供至关重要的培训方面。
结论
这些研究和许多其他正在进行的研究表明,国际合作在解决重大全球性问题方面具有强大的力量。实时开放的数据共享使研究小组能够迅速地在发现的基础上进行构建,而基于片段的筛选和计算对接方法等开拓性新技术的使用已经彻底改变了我们的新药发现方法。
确认:
Frank von Delft, Alice Douangamath, Ailsa Powell, Alex Dias, Louise Dunnett, Jose brandado - neto, Anthony Aimon, Rachael Skyner, Tyler gorley - stone, Warren Thompson, Conor Wild, Anna Carberry, Elliot Nelson, Felicity Bertram, Lizbe Koekemoer, Mike Fairhead, Tobias Krojer, Ruben Sanchez-Garcia, Martin Walsh, David Owen, Petra Lukacik, Claire strine - damerell, Halina Mikolajek, Opher Gileadi, Joseph Newman, Yuliana Yosaatmadja, Andre Godoy, Leo James, Jakub Luptak, Marion Schuller, Ivan Ahel,James Fraser, Brian Shoichet, Galen Correy, Stefan Gahbauer, COVID登月联盟,QCRG结构生物学联盟,钻石光源的工作人员。
参考文献
1.v代尔夫特F.翻译科学家2016 - https://thetranslationalscientist.com/research-field/fragment-screening-at-almost-the-speed-of-light
2.2019冠状病毒登月联盟,2020 https://www.biorxiv.org/content/10.1101/2020.10.29.339317v1
3.PostEra网站https://covid.postera.ai/covid
4.Douangamath, A.等人。SARS-CoV-2主要蛋白酶的晶体学和亲电片段筛选。Nat. common . 2020 - https://doi.org/10.1038/s41467-020-18709-w
5.张志强,张志强,张志强,等。科学进展2021;7:DOI: 10.1126/sciadv.abf8711